由极性键形成的分子一定是极性分子吗
由极性键形成的(双原子)分子一定是极性分子。
解析:
因为是双原子分子,两原子间的化学键有极性,此分子就一定有极性了。如果是三原子以上的多原子分子,那就不一定了。
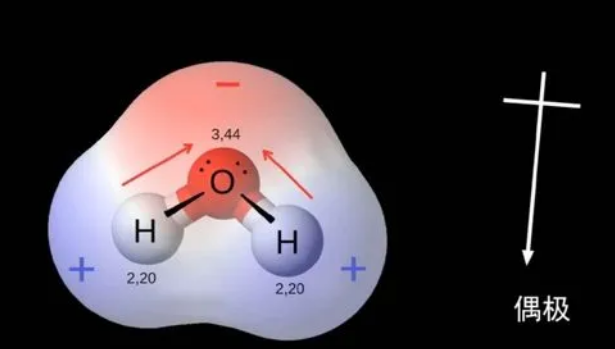
分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的、不对称的,这样的分子为极性分子,以极性键结合的双原子分子一定为极性分子,极性键结合的多原子分子视结构情况而定,如CH4就不是极性分子。
非极性分子的判断:
1、化合价法
组成为ABn型化合物,若中心原子A的化合价等于族的序数,则该化合物为非极性分子。如:CH4、CCl4、SO3、PCl5等。
2、受力分析法
若已知键角(或空间结构),可进行受力分析,合力为0者为非极性分子。如:CO2、C2H4、BF3等。
同种原子组成的双原子分子都是非极性分子。
不是非极性分子的就是极性分子。